terça-feira, 9 de dezembro de 2008
Glossário (Resumão)
Aterosclerose: doença das artérias, causada pelo depósito de placas de gordura.
Angina: dor no peito.
Colesterol: apesar de ser chamado de gordura, na verdade quimicamente é um álcool. Essa substância circula pelo sangue acoplado a moléculas de lipoproteínas.
Coronária: as artérias que irrigam o coração.
Dislipidemia: qualquer alteração nos níveis dos lipídios no sangue, como colesterol e triglicérides.
Eletrocardiograma: exame que registra a atividade elétrica do coração.
Hiperlipidemia: aumento das taxas de lipídios no sangue.
Hipercolesterolemia: aumento das taxas de colesterol no sangue.
Infarto: morte do músculo cardíaco por falta de irrigação.
Isquemia: situação em que ocorre falta de oxigenação em um órgão ou tecido.
LDL: sigla em inglês para lipoproteína de baixa densidade (low density lipoprotein), o famoso mau colesterol. Em excesso no sangue, se deposita na parede das artérias.
http://www.minhavida.com.br/MostraMateriaSaude.vxlpub?codMateria=1482
quinta-feira, 27 de novembro de 2008
Alcachofra
Aveia
Azeite
Chá
Farelos e cereais integrais
Laranja
Oleaginosas
Peixe
Soja
Vinho
Então, mãos na massa!!
Fonte: http://paginas.terra.com.br/esporte/capoeiradabahia/medicina/ass_med_colesterol.htm
quinta-feira, 20 de novembro de 2008
terça-feira, 18 de novembro de 2008
Patologias
O termo arteriosclerose significa, literalmente, "endurecimento das artérias", mas é usado para indicar um grupo de processos que tem em comum o espessamento da parede arterial e a perda de elasticidade da mesma.
 Essa deficiência causa inúmeras conseqüências para o indivíduo que a possui. São indicadas com este termo três variantes morfológicas: a aterosclerose, caracterizada pela formação de ateromas (depósitos circunscritos de lipídeos na camada íntima); esclerose calcificante da média ou esclerose de Mönckberg, que consiste na calcificação da camada média das artérias musculares principalmente, mas também das grandes artérias, de modo geral não diminui a luz arterial, porém pode facilitar o desenvolvimento de aneurismas; e a arteriosclerose, que é devido a uma proliferação fibromuscular ou endotelial, causando portanto um espessamento da parede das pequenas artérias e arteríolas. Nos deteremos a uma doença da classe da arteriosclerose chamada aterosclerose. Em um indivíduo, em vasos diferentes ou em um mesmo vaso, podem ocorrer duas ou três destas variantes. Como a aterosclerose é de longe a forma mais comum e importante de arteriosclerose, os termos são usados indiferentemente. A aterosclerose é uma doença das artérias de grande e médio calibre, caracterizada por depósitos lipídicos e espessamento da camada íntima, com rompimento da camada média. Comumente, há o comprometimento da aorta, seu ramos principais como as ilíacas, femorais e carótidas, e as artérias que suprem o coração e o cérebro. Caracteristicamente, a aterosclerose interfere de modo progressivo ou súbito no fluxo sangüíneo, e é a principal causa de morte nos Estados Unidos. As mortes causadas por doença vascular, mais especificamente por infarto do miocárdio e por acidente vascular cerebral, são mais numerosas do que as duas causas subseqüentes, câncer e acidentes combinados. A aterosclerose, como já mencionado, é uma doença multifatorial, ou seja, é conseqüência de uma série de fatores. Os fatores que mais claramente têm sido implicados são o colesterol, o fumo e a hipertensão. Outros importantes fatores predisponentes são os triglicerídios do soro, o diabetes e a obesidade. A obesidade infantil é outro fato que tem preocupado especialistas e pais. Acontece com maior freqüência no primeiro ano e após o oitavo ano de vida, é predominante nas famílias de renda maior (11,3 %) do que naquelas de menor renda (5,3 %). Mas, em qualquer faixa sócio-econômica, os padrões de vida atuais em que as ruas não são um lugar seguro de se estar, as crianças acabam por passar o dia em frente a tv, computador, vídeo game ou brincando em atividades que não exijam tanto espaço e energia. Pesquisas têm revelado que 26% das crianças americanas, entre 8 e 16 anos, passam 4 ou mais horas em frente à televisã
Essa deficiência causa inúmeras conseqüências para o indivíduo que a possui. São indicadas com este termo três variantes morfológicas: a aterosclerose, caracterizada pela formação de ateromas (depósitos circunscritos de lipídeos na camada íntima); esclerose calcificante da média ou esclerose de Mönckberg, que consiste na calcificação da camada média das artérias musculares principalmente, mas também das grandes artérias, de modo geral não diminui a luz arterial, porém pode facilitar o desenvolvimento de aneurismas; e a arteriosclerose, que é devido a uma proliferação fibromuscular ou endotelial, causando portanto um espessamento da parede das pequenas artérias e arteríolas. Nos deteremos a uma doença da classe da arteriosclerose chamada aterosclerose. Em um indivíduo, em vasos diferentes ou em um mesmo vaso, podem ocorrer duas ou três destas variantes. Como a aterosclerose é de longe a forma mais comum e importante de arteriosclerose, os termos são usados indiferentemente. A aterosclerose é uma doença das artérias de grande e médio calibre, caracterizada por depósitos lipídicos e espessamento da camada íntima, com rompimento da camada média. Comumente, há o comprometimento da aorta, seu ramos principais como as ilíacas, femorais e carótidas, e as artérias que suprem o coração e o cérebro. Caracteristicamente, a aterosclerose interfere de modo progressivo ou súbito no fluxo sangüíneo, e é a principal causa de morte nos Estados Unidos. As mortes causadas por doença vascular, mais especificamente por infarto do miocárdio e por acidente vascular cerebral, são mais numerosas do que as duas causas subseqüentes, câncer e acidentes combinados. A aterosclerose, como já mencionado, é uma doença multifatorial, ou seja, é conseqüência de uma série de fatores. Os fatores que mais claramente têm sido implicados são o colesterol, o fumo e a hipertensão. Outros importantes fatores predisponentes são os triglicerídios do soro, o diabetes e a obesidade. A obesidade infantil é outro fato que tem preocupado especialistas e pais. Acontece com maior freqüência no primeiro ano e após o oitavo ano de vida, é predominante nas famílias de renda maior (11,3 %) do que naquelas de menor renda (5,3 %). Mas, em qualquer faixa sócio-econômica, os padrões de vida atuais em que as ruas não são um lugar seguro de se estar, as crianças acabam por passar o dia em frente a tv, computador, vídeo game ou brincando em atividades que não exijam tanto espaço e energia. Pesquisas têm revelado que 26% das crianças americanas, entre 8 e 16 anos, passam 4 ou mais horas em frente à televisã o e que favorece o desenvolvimento da obesidade. Dentre os fatores que predispõem a obesidade encontra-se o fator endócrino, estando envolvido, principalmente, o hormônio leptina. A leptina é um hormônio feito pelas células que armazenam gordura e que sinaliza ao cérebro que iniba a fome da pessoa, em ratos que não conseguem produzir este hormônio ocorre a obesidade, portanto, comportamento semelhante ocorre nos humanos.
o e que favorece o desenvolvimento da obesidade. Dentre os fatores que predispõem a obesidade encontra-se o fator endócrino, estando envolvido, principalmente, o hormônio leptina. A leptina é um hormônio feito pelas células que armazenam gordura e que sinaliza ao cérebro que iniba a fome da pessoa, em ratos que não conseguem produzir este hormônio ocorre a obesidade, portanto, comportamento semelhante ocorre nos humanos.Possíveis Soluções para a Patologia
O controle da regulação metabólica de qualquer via normalmente é obtido pela modulação da atividade de uma enzima fundamental. – conhecida como enzima controlada. Esta enzima freqüentemente catalisa o passo principal – o primeiro que pode ser identificado como regulador daquela via. E é extremamente interessante que o controle da biossíntese do colesterol ocorra numa fase relativamente inicial do processo, tendo como substrato a enzima a que utiliza uma molécula com 6 átomos de carbono. A HMG-CoA redutase é a enzima taxa-limitante que catalisa a etapa comprometida que resulta na produção do ácido mevalônico. A síntese hepática de HMG-CoA redutase é estimulada pelo jejum e inibida pelo colesterol ingerido na dieta. A atividade da HMG-CoA é controlada pela modificação covalente induzida pela retroalimentação do colesterol e por vários hormônios metabólicos. A indústria farmacêutica investe milhões de dólares na pesquisa de fármacos capazes de reduzir o nível de colesterol. Por exemplo, o fármaco Citalor inibe a HMG-CoA redutase no local de síntese do colesterol. Isso promove uma redução da síntese hepática do colesterol e uma contra regulação compensatória dos receptores LDL hepáticos, que extraem partículas de LDL do plasma e a introduz nas células hepáticas para degradação e reprocessamento do seu colesterol. Isto, finalmente, resulta em aumento da captação e metabolismo de LDL-C circulantes. Algumas plantas reagem a organismos patogênicos, predadores, produzindo substâncias chamadas fitoalexínas. O fármaco Resveratrol (trans-3,5,4'-trihidroxistilbeno) é uma fitoalexína sintetizada por muitas plantas, e é encontrado, em grande escala, nas cascas da uva, como uma resposta à invasão por fungos do tipo Botrytis cinerea. Muitos cientistas já publicaram trabalhos mostrando uma ligação entre o consumo de vinho tinto e a diminuição das doenças cardiovasculares - o chamado "French Paradox". A estrutura química do resveratrol é semelhante ao estrógeno sintético dietilestilbestrol (DES). Cientistas acreditam que o resveratrol pode, assim como o DES, elevar a concentração de HDL sanguíneo - o "bom colesterol".
Dentre as doenças decorrentes da aterosclerose tem-se:
INFARTO

Dados do Instituto do Coração mostram que cerca de 40% dos pacientes de doenças coronarianas não apresentam os chamados fatores clássicos de risco. A ocorrência é mais preocupante quando se sabe que as doenças cardiovasculares são a primeira causa de morte no Brasil, 33% do total. De cada dez vítimas, seis, em média, são do sexo masculino. O infarto do miocárdio ou ataque cardíaco consiste em uma lesão no músculo cardíaco causada pela obstrução da artéria coronária, responsável pela irrigação do coração. Quando a artéria entope, parte do músculo cardíaco (miocárdio) deixa de receber sangue e nutrientes. Cerca de 20 minutos depois, essa privação mata os tecidos da região atingida. Quanto maior a artéria bloqueada, maior a área afetada. Mesmo que o coração esteja saudável, uma obstrução no trajeto, dependendo do tamanho, pode fazê-l
 o diminuir o ritmo de bombeamento do sangue, provocando desde angina (dor no peito) até a morte súbita. Dentre os principais sintomas estão: dor ou forte pressão no peito; dor no peito refletindo nos ombros, braço esquerdo (ou os dois) pescoço e maxilar; dor abdominal; suor, palidez, falta de ar, perda temporária de consciência, sensação de morte eminente; náuseas e vômitos. Analisando a população, em geral, há fatores que potencializam certos grupos a um infarto. Dentre esses fatores, pode-se citar: o histórico familiar de doença coronariana; a idade (a partir dos 60 anos); o colesterol alto (desregulado); os triglicérides elevado; a hipertensão arterial; a obesidade; o diabetes; o fumo; o estresse; e o sedentarismo. Vale lembrar que o único fator que não pode ser alterado e/ou tratado é a pré-disposição familiar.
o diminuir o ritmo de bombeamento do sangue, provocando desde angina (dor no peito) até a morte súbita. Dentre os principais sintomas estão: dor ou forte pressão no peito; dor no peito refletindo nos ombros, braço esquerdo (ou os dois) pescoço e maxilar; dor abdominal; suor, palidez, falta de ar, perda temporária de consciência, sensação de morte eminente; náuseas e vômitos. Analisando a população, em geral, há fatores que potencializam certos grupos a um infarto. Dentre esses fatores, pode-se citar: o histórico familiar de doença coronariana; a idade (a partir dos 60 anos); o colesterol alto (desregulado); os triglicérides elevado; a hipertensão arterial; a obesidade; o diabetes; o fumo; o estresse; e o sedentarismo. Vale lembrar que o único fator que não pode ser alterado e/ou tratado é a pré-disposição familiar.Há medidas de prevenção que corroboram para diminuir os riscos. Por exemplo, a alimentação balanceada, manter o peso sob controle, a prática de exercícios regularmente e, além disso, realizar exames de prevenção periodicamente (avaliação medica, eletrocardiograma, hemograma, colesterolemia, triglicérides, glicemia e teste de esforço). O cardiologista opta pela desobstrução mecânica quando essa acarreta benefícios mais imediatos ao paciente. Nem sempre existe, na sala de atendimento, o equipamento necessário para fazer cateterismo e atender a imensa população que apresenta doenças cardiovasculares, já que elas acometem milhões de pessoas por ano no mundo todo. Por outro lado, o tratamento farmacológico é uma solução que também apresenta bons resultados nos casos de infarto do miocárdio. Basicamente, consiste em ministrar uma droga, isto é, uma substância com a propriedade de dissolver o coágulo antes que o músculo cardíaco seja irreversivelmente destruído. Alguns especialistas optam pela angioplastia que trata-se de uma técnica simples que consiste no seguinte: o paciente é deitado numa cama de exames que tem embaixo um aparelho de raio-X e acima, uma câmera. Por uma incisão na virilha ou no braço, introduz-se um tubo plástico na origem da artéria coronária, através da qual ele é conduzido até alcançar a artéria que irriga o coração. O contraste que se injeta, a seguir, torna visível a árvore coronária e o lugar exato em que se deu a obstrução. Daí em diante, esse cateter funciona como guia para conduzir um fiozinho flexível e delgado que ultrapassa a obstrução e que será recoberto por outro cateter em cuja extremidade existe um pequeno balão inflável. Utilizando uma bomba pneumática, o balão é insuflado no local em que ocorreu o entupimento para comprimir a placa gordurosa e os trombos contra a parede da artéria.

ACIDENTE VASCULAR CEREBRAL (AVC)
O acidente vascular cerebral (AVC), conhecido popularmente como derrame cerebral, pode ser de dois tipos: 1 - acidente vascular isquêmico que é a falta de circulação numa área do cérebro provocada por obstrução de uma ou mais artérias por ateromas, trombose ou embolia. Ocorre, em geral, em pessoas mais velhas, com diabetes, colesterol elevado, hipertensão arterial, problemas vasculares e fumantes; ou, 2 - acidente vascular hemorrágico que consiste em um sangramento cerebral
 provocado pelo rompimento de uma artéria ou vaso sangüíneo, em virtude de hipertensão arterial, problemas na coagulação do sangue, traumatismos. Pode ocorrer em pessoas mais jovens e a evolução é mais grave. Dentre os sintomas do acidente vascular isquêmico pode-se citar: a perda repentina da força muscular e/ou da visão, dificuldade de comunicação oral, tonturas, formigamento num dos lados do corpo e alterações da memória. Algumas vezes, esses sintomas podem ser transitórios – ataque isquêmico transitório (AIT). Mas nem por isso deixam de exigir cuidados médicos imediatos. E, para o acidente vascular hemorrágico, tem-se: dor de cabeça, edema cerebral, aumento da pressão intracraniana, náuseas e vômitos e déficits neurológicos semelhantes aos provocados pelo acidente vascular isquêmico. Portanto, nem sempre diferenciar os acidentes vasculares é fácil, por isso procurar atendimento médico é imprescindível. Vale lembrar que há fatores de riscos de uma pessoa vir a ter um AVC. Além disso, os mesmos comportamentos que potencializam o AVC potencializam, também, ataques cardíacos. São eles: hipertensão arterial, colesterol elevado, fumo, diabetes, histórico familiar, ingestão de álcool, vida sedentária, excesso de peso e o estresse. O acidente vascular cerebral é uma emergência médica, portanto o paciente deve ser encaminhado imediatamente para atendimento hospitalar. Trombolíticos e anticoagulantes (impedem a coagulação sangüínea) podem diminuir a extensão dos danos no caso de acidentes isquêmicos. A cirurgia pode estar indicada para a retirada de coágulos nos acidentes hemorrágicos ou para a retirada de embolos obstrutivos (coágulos que impedem a passagem regular do sangue) nos acidentes isquêmicos. Existem recursos terapêuticos capazes de ajudar a restaurar funções, movimentos e fala e, quanto antes começarem a ser aplicados, melhores serão os resultados. Controle a pressão arterial e o nível de açúcar no sangue. Hipertensos e diabéticos exigem tratamento e precisam de acompanhamento médico permanente Controlando a pressão arterial e o nível de açúcar no sangue, respectivamente. Pessoas com pressão e glicemia normais raramente têm derrames. É interessante, também, procurar manter abaixo de 200 o índice do coleste
provocado pelo rompimento de uma artéria ou vaso sangüíneo, em virtude de hipertensão arterial, problemas na coagulação do sangue, traumatismos. Pode ocorrer em pessoas mais jovens e a evolução é mais grave. Dentre os sintomas do acidente vascular isquêmico pode-se citar: a perda repentina da força muscular e/ou da visão, dificuldade de comunicação oral, tonturas, formigamento num dos lados do corpo e alterações da memória. Algumas vezes, esses sintomas podem ser transitórios – ataque isquêmico transitório (AIT). Mas nem por isso deixam de exigir cuidados médicos imediatos. E, para o acidente vascular hemorrágico, tem-se: dor de cabeça, edema cerebral, aumento da pressão intracraniana, náuseas e vômitos e déficits neurológicos semelhantes aos provocados pelo acidente vascular isquêmico. Portanto, nem sempre diferenciar os acidentes vasculares é fácil, por isso procurar atendimento médico é imprescindível. Vale lembrar que há fatores de riscos de uma pessoa vir a ter um AVC. Além disso, os mesmos comportamentos que potencializam o AVC potencializam, também, ataques cardíacos. São eles: hipertensão arterial, colesterol elevado, fumo, diabetes, histórico familiar, ingestão de álcool, vida sedentária, excesso de peso e o estresse. O acidente vascular cerebral é uma emergência médica, portanto o paciente deve ser encaminhado imediatamente para atendimento hospitalar. Trombolíticos e anticoagulantes (impedem a coagulação sangüínea) podem diminuir a extensão dos danos no caso de acidentes isquêmicos. A cirurgia pode estar indicada para a retirada de coágulos nos acidentes hemorrágicos ou para a retirada de embolos obstrutivos (coágulos que impedem a passagem regular do sangue) nos acidentes isquêmicos. Existem recursos terapêuticos capazes de ajudar a restaurar funções, movimentos e fala e, quanto antes começarem a ser aplicados, melhores serão os resultados. Controle a pressão arterial e o nível de açúcar no sangue. Hipertensos e diabéticos exigem tratamento e precisam de acompanhamento médico permanente Controlando a pressão arterial e o nível de açúcar no sangue, respectivamente. Pessoas com pressão e glicemia normais raramente têm derrames. É interessante, também, procurar manter abaixo de 200 o índice do coleste rol total. Às vezes, só se consegue esse equilíbrio com medicamentos. Não os tome nem deixe de tomá-los por conta própria. Ouça sempre a orientação de um médico. Adote uma dieta equilibrada, reduzindo a quantidade de açúcar, gordura, sal e bebidas alcoólicas. Não fume. Está provado que o cigarro é um fator de alto risco para acidentes vasculares. Estabeleça um programa regular de exercícios físicos. Faça caminhadas de 30 minutos diariamente. Informe seu médico se em sua família houver casos doenças cardíacas e neurológicas como o AVC. Procure distrair-se para reduzir o nível de estresse. Encontre os amigos, participe de atividades culturais, comunitárias, etc.
rol total. Às vezes, só se consegue esse equilíbrio com medicamentos. Não os tome nem deixe de tomá-los por conta própria. Ouça sempre a orientação de um médico. Adote uma dieta equilibrada, reduzindo a quantidade de açúcar, gordura, sal e bebidas alcoólicas. Não fume. Está provado que o cigarro é um fator de alto risco para acidentes vasculares. Estabeleça um programa regular de exercícios físicos. Faça caminhadas de 30 minutos diariamente. Informe seu médico se em sua família houver casos doenças cardíacas e neurológicas como o AVC. Procure distrair-se para reduzir o nível de estresse. Encontre os amigos, participe de atividades culturais, comunitárias, etc.TROMBOSE
Quando sofremos um corte, o sangue escorre um pouco e pára, porque o corpo humano é dotado de um sistema de coagulação altamente eficaz. As plaquetas (fragmentos celulares presente no sangue), por exemplo, convergem para o local do ferimento e formam um trombo (espécie de placa protetora) para bloquear o sangramento. Decorrido algum tempo, esse trombo se dissolve, o vaso é recanalizado e a circulação volta ao normal. Há pessoas que apresentam distúrbios de hemostasia (conjunto de mecanismos que o organismo emprega para coibir hemorragia) e formam trombos (coágulos) num lugar onde não houve sangramento. Em geral, eles se formam nos membros inferiores. Como sua estrutura é sólida e amolecida, um fragmento pode desprender-se e seguir o trajeto da circulação venosa que retorna aos pulmões para o sangue ser oxigenado. Nos pulmões, conforme o tamanho do trombo, pode ocorrer um entupimento – a embolia pulmonar – uma complicação grave que pode causar morte súbita
 . A trombose pode ser completamente assintomática ou apresentar sintomas como dor, inchaço e aumento da temperatura nas pernas, coloração vermelho-escura ou arroxeada e, até, endurecimento da pele. Dentre as principais causas pode-se citar: imobilidade provocada por prolongadas internações hospitalares, síndrome da classe econômica (como também é conhecida) que ocorre devido à dificuldade de movimentação durante viagens longas em aviões e ônibus. Pode ocorrer, também, devido a terapia de reposição hormonal, uso de anticoncepcionais e cirurgias. Alguns fatores como predisposição genética, idade mais avançada, colesterol elevado, cirurgias e hospitalizações prolongadas, obesidade, uso de anticoncepcionais, consumo de álcool, fumo(O cigarro aumenta as chances porque seus componentes lesam veias e artérias. Lesões essas que podem gerar acúmulo plaquetário e acarretar trombos), falta de movimentação, aumentam o risco de desenvolver trombose. A fim de evitar a trombose realizar caminhadas, vestir meias elásticas, massagear a panturrilha sempre que for ficar sentado por muito tempo ajuda, e muito. Em caso de suspeita procurar atendimento médico e não se auto medicar é fundamental. Existem medicamentos para reduzir a viscosidade do sangue e dissolver o coágulo (anticoagulantes) que ajudam a diminuir o risco, a evitar a ocorrência de novos episódios e o aparecimento de seqüelas, mas que só devem ser usados mediante prescrição médica depois de criteriosa avaliação. Massageadores pneumáticos intermitentes também podem ser usados nesses casos.
. A trombose pode ser completamente assintomática ou apresentar sintomas como dor, inchaço e aumento da temperatura nas pernas, coloração vermelho-escura ou arroxeada e, até, endurecimento da pele. Dentre as principais causas pode-se citar: imobilidade provocada por prolongadas internações hospitalares, síndrome da classe econômica (como também é conhecida) que ocorre devido à dificuldade de movimentação durante viagens longas em aviões e ônibus. Pode ocorrer, também, devido a terapia de reposição hormonal, uso de anticoncepcionais e cirurgias. Alguns fatores como predisposição genética, idade mais avançada, colesterol elevado, cirurgias e hospitalizações prolongadas, obesidade, uso de anticoncepcionais, consumo de álcool, fumo(O cigarro aumenta as chances porque seus componentes lesam veias e artérias. Lesões essas que podem gerar acúmulo plaquetário e acarretar trombos), falta de movimentação, aumentam o risco de desenvolver trombose. A fim de evitar a trombose realizar caminhadas, vestir meias elásticas, massagear a panturrilha sempre que for ficar sentado por muito tempo ajuda, e muito. Em caso de suspeita procurar atendimento médico e não se auto medicar é fundamental. Existem medicamentos para reduzir a viscosidade do sangue e dissolver o coágulo (anticoagulantes) que ajudam a diminuir o risco, a evitar a ocorrência de novos episódios e o aparecimento de seqüelas, mas que só devem ser usados mediante prescrição médica depois de criteriosa avaliação. Massageadores pneumáticos intermitentes também podem ser usados nesses casos.Dica: A fim de prevenir qualquer doença coronariana ou degenarativa, além das citadas, não é uma tarefa difícil. Como já foi dito, além de atividades físicas regulares acompanhadas por um profissional qualificado é interessante que o indivíduo tenha alimentação saudável (reeducação alimentar), ou seja, balanceada, na qual ele coma de tudo mas com moderação. Realizar exames periodicamente
 também corrobora para manter os níveis corporais regulados, já que o médico estará acompanhando a progressão corporal. Para pacientes com doenças que são apenas controladas, como diabetes e hipertensão, as recomendações são mais rigorosas mas não são impossíveis de serem administradas. Que fique claro que as medidas citadas tem por objetivo a prevenção e não a segurança de nunca sofrer de uma doença, principalmente do coração.
também corrobora para manter os níveis corporais regulados, já que o médico estará acompanhando a progressão corporal. Para pacientes com doenças que são apenas controladas, como diabetes e hipertensão, as recomendações são mais rigorosas mas não são impossíveis de serem administradas. Que fique claro que as medidas citadas tem por objetivo a prevenção e não a segurança de nunca sofrer de uma doença, principalmente do coração.* http://www.plantamed.com.br/DIV/Infarto_do_miocardio.htm * http://drauziovarella.ig.com.br/arquivo/arquivo.asp?doe_id=49 *http://www.drashirleydecampos.com.br/noticias.php?noticiaid=3261&assunto=Farm%C3%A1cia,%20bioqu%C3%ADmica,fisiologia * http://www.ucs.br/ccet/defq/naeq/material_didatico/textos_interativos_09.htm *http://portal.saude.gov.br/portal/aplicacoes/noticias/noticias_detalhe.cfm?co_seq_noticia=51557
" Concentração do Colesterol regula, indiretamente, a sua síntese"
Mecanismos acionados em condições de alto conteúdo de colesterol intracelular:
Repressão de genes que codificam enzimas da via de síntese de colesterol, sendo a HMG-CoA redutase a de maior expressão. A enzima, a exemplos de outras enzimas que fazem parte da via de biossíntese, é inibida por fosforilação catalisada pela proteína quinase dependente de AMP(AMPK), que por sua vez é ativada pelo glucagon. Já a insulina promove a desfosforilação, promovendo a síntese de colesterol;
Repressão do gene do receptor de LDL. A uma diminuição do número de receptores de LDL propicia uma redução no aporte de colesterol para as células;
Indução de genes relacionados ao transporte reverso de colesterol, portanto ocorre um transporte do excesso de colesterol dos tecidos periféricos para o fígado na forma de HDL, cujo nível aumenta;
Indução de genes envolvidos com a excreção de colesterol, por exemplo, genes de enzimas reguladoras da via de síntese de sais biliares, propiciando a conversão de colesterol em sais biliares, ou seja, a sua exceção.
A repressão e a indução são feita através dos oxiesteróides. Os oxiesteróides são esteróides derivados do colesterol por incorporação de oxigênio na cadeia lateral, eles atuam como moduladores da expressão gênica. Existem sensores dos níveis elevados de oxiesteróides e conseqüentemente do colesterol, determinados receptores nucleares. A interação com os oxiesteróides leva à ativação destes receptores, que atuam como fatores de transcrição, ligando-se ao promotor dos genes-alvo; são capazes de regular a expressão gênica negativa ou positivamente6.
Nos mamíferos a produção do colesterol é regulada pela concentração de colesterol intracelular e pelos hormônios glucagon e insulina. O passo limitante na via para colesterol é a conversão do HMG-CoA em mevalonato, a HMG-CoA redutase, a enzima que catalisa essa reação, é uma enzima reguladora cuja atividade pode sofrer variações de mais de 100 vezes. Uma das formas de se beneficiar dessas variações para o controle da alta concentração de colesterol no sangue é por meio das estatinas.
Estatinas
De forma geral, as estatinas causam redução dos níveis de triglicerídeos, mas este efeito parece ser observado apenas em pacientes hipertrigliceridêmicos. Os valores praticamente constantes obtidos da relação triglicerídeos/LDL - colesterol, nestes estudos, mostram que quanto maior a atividade de estatina para diminuir o LDL - colesterol, maior será o efeito na diminuição dos níveis de triglicerídeos7. A diminuição de colesterol plasmático é acompanhada pela redução dos níveis de LDL.
Apesar da importância deste mecanismo no efeito hipocolesterolêmico, as estatinas também induzem o aumento de receptores LDL, onde a lipoproteína LDL se fixa no tecido hepático, ocorrendo depuração de partículas com apo B-100, por endocitose. O aumento de atividade dos receptores de LDL hepático é um dos fatores mais importantes para diminuição dos níveis de LDL plasmático. Por esta razão os inibidores de HMG-CoA redutase possuem dupla ação, diminuem a biossíntese de colesterol e causam aumento do número de receptores LDL hepático, aumentando a remoção de IDL e LDL circulantes. Mevastatina (ou compactina) foi o primeiro inibidor de HMG-CoA redutase descoberto em 1976, originalmente isolado como produto metabólico de culturas de Penicillium citrinium5, sendo sua afinidade pelo sítio enzimático cerca de 10.000 vezes superior ao substrato HMG-CoA. Por outro lado, lovastatina (ou mevinolina) foi isolada posteriormente de culturas de Aspergillus terreus e Monascus ruber com estrutura semelhante à mevastatina (grupo 6´-metílico adicional), mas com potência superior. Em 1987 lovastatina foi aprovada pelo FDA para uso terapêutico, enquanto mevastatina foi abandonada devido a problemas na morfologia intestinal de cachorros e toxicidade hepatocelular verificada em ratos. A introdução de novos derivados sintéticos da classe das estatinas ocorreu em 1996 e 1997, com atorvastatina (Lipitor) e cerivastatina (Baycon), respectivamente. No entanto, em agosto de 2001, a Bayer retirou cerivastatina do mercado devido à incidência de mais de 100 casos de rabdomiólise fatal, relacionados a dano severo da musculatura esquelética com alteração das células musculares, liberação de mioglobina e, freqüentemente, acompanhado de problemas renais12. A maioria dos casos foi observada em tratamentos com doses excessivas de cerivastatina ou em doses normais associadas ao uso de genfibrosil, fármaco da classe dos fibratos empregados no tratamento das hipertrigliceridemias1. Em 2002, atorvastatina foi o fármaco mais vendido no mundo, rendendo para o fabricante Pfizer cerca de US$ 8 bilhões10,13. Rosuvastatina (Astra Zeneca), aprovada em agosto de 2003 pelo FDA, deverá concorrer por este mercado, enquanto pitavastatina, nova estatina sintética em estudos pela empresa japonesa Kowa Company, apresentou grande eficácia em reduzir os níveis de colesterol, com doses diárias de 1 a 4 mg e ação similar ou superior à atorvastatina2,8.
No momento, seis estatinas são empregadas clinicamente: lovastatina (Mevacor), pravastatina (Pravachol), sinvastatina (Zocor) e fluvastatina (Lescol), primeiro agente totalmente sintético, derivado de mevalonolactona produzido na forma racêmica11. A nova geração de estatinas sintéticas, enantiomericamente puras, é representada por atorvastatina (Lipitor) e rosuvastatina (Crestor).
Os efeitos colaterais não são freqüentes, mas um dos mais sérios está relacionado à ação hepatotóxica, com possível aumento das enzimas aspartato e alanina transaminases. Miopatias, com evolução a rabdomiólises e insuficiência renal, são raras, mas são efeitos graves associados ao uso de estatinas. Parece que o uso concomitante de estatinas com eritromicina, ciclosporina, niacina e fibratos aumenta o risco de miopatias em 10-30% dos pacientes.
Niacina
 Os fibratos constituem um grupo de drogas hipolipemiantes, derivadas do ácido fíbrico, dos quais o clofibrato foi inicialmente utilizado a partir de 1962(14). Análogos ao clofibrato foram a seguir introduzidos na prática médica: bezafibrato, etofibrato, fenofibrato e ciprofibrato.
Os fibratos constituem um grupo de drogas hipolipemiantes, derivadas do ácido fíbrico, dos quais o clofibrato foi inicialmente utilizado a partir de 1962(14). Análogos ao clofibrato foram a seguir introduzidos na prática médica: bezafibrato, etofibrato, fenofibrato e ciprofibrato. -Menor fluxo de ácidos graxos livres para o fígado;
-Menor síntese hepática de VLDL;
-Estímulo à atividade da lipase lipoprotéica;
-Aumento da excreção biliar de colesterol hepático.
Resinas de Trocas de Ácidos Biliares

Exercícios Físicos e hábitos Alimentares

 Relacionando os hábitos alimentares tem-se a coordenadora de Nutrição do Hospital do Coração, em São Paulo, Cyntia Carla da Silva, que desfaz o mito da carne vermelha versus a branca. O importante não é a cor ou a procedência, mas o corte. O filé mignon e o lombo suíno, por exemplo, são mais saudáveis do que a picanha bovina. Assim como a coxa e a asa do frango com pele podem ser tão prejudiciais à saúde quanto o cupim gorduroso. É preciso considerar também a quantidade ingerida. “Tem gente que acha que o filé de frango é a salvação da lavoura, aí come dois filés enormes no almoço. É lógico que não vai adiantar nada”, diz Cyntia Carla da Silva(15).
Relacionando os hábitos alimentares tem-se a coordenadora de Nutrição do Hospital do Coração, em São Paulo, Cyntia Carla da Silva, que desfaz o mito da carne vermelha versus a branca. O importante não é a cor ou a procedência, mas o corte. O filé mignon e o lombo suíno, por exemplo, são mais saudáveis do que a picanha bovina. Assim como a coxa e a asa do frango com pele podem ser tão prejudiciais à saúde quanto o cupim gorduroso. É preciso considerar também a quantidade ingerida. “Tem gente que acha que o filé de frango é a salvação da lavoura, aí come dois filés enormes no almoço. É lógico que não vai adiantar nada”, diz Cyntia Carla da Silva(15).  Apenas um trabalho comparou a quantidade de colesterol nos diferentes tipos de carne por meio de cromatografia, concluindo que o frango tinha maior quantidade de colesterol que a carne de vaca (exceto fígado) e de porco. Entretanto, não foi testado o efeito no perfil lipídico9. O cardiologista Raul Dias dos Santos Filho diz que a única forma de se livrar do mau colesterol é mudar os hábitos. Equilibrar a alimentação, parar de fumar e fazer exercícios físicos são itens obrigatórios para quem quer garantir uma vida longa e de qualidade. “Não precisa ficar neurótico. Na alimentação, não há nada proibido, mas é preciso bom senso(16).
Apenas um trabalho comparou a quantidade de colesterol nos diferentes tipos de carne por meio de cromatografia, concluindo que o frango tinha maior quantidade de colesterol que a carne de vaca (exceto fígado) e de porco. Entretanto, não foi testado o efeito no perfil lipídico9. O cardiologista Raul Dias dos Santos Filho diz que a única forma de se livrar do mau colesterol é mudar os hábitos. Equilibrar a alimentação, parar de fumar e fazer exercícios físicos são itens obrigatórios para quem quer garantir uma vida longa e de qualidade. “Não precisa ficar neurótico. Na alimentação, não há nada proibido, mas é preciso bom senso(16).2. Kajinami, K.; Takekoshi, N.; Saito, Y; Cardiovasc. Drug Rev. 2003, 21, 199.
3. Lea, A. P.; McTavish, D.; Drugs 1997, 53, 828.
4. Leitersdorf, E.; Br. J. Clin. Pract. 1994, Suppl. 77, 24.
5. Liao, J. K.; Laufs, U.; Annu. Rev. Pharmacol. Toxicol. 2005, 45, 89.
6. Marzzoco, Anita p. 300, 301
7. Mukai, Y.; Shimokawa, H.; Matoba, T.; Hiroki, J.; Kunihiro, I.; Fujiki, T.; Takeshita, A.; J. Cardiol. Pharmacol. 2003, 42, 118.
8. Mukhtar, R. Y. A.; Reid, J.; Reckless, J. P. D.; Int. J. Clin. Pract. 2005, 59, 239.
9. Rowe A, Bertoni AS, Pereira PL, Matsushita M, Souza, NE; Cholesterol in
Beef, Pork, Chicken and Their Products Commercialized in Maringa,
Paraná, Brasil. Arch Lati Noam Nutr, 1997 Sep; 47(3): 282-4
10. Ver "Editorial", The statin wars: why AstraZeneca must retreat, The Lancet 2003, 362 (9393), 1341.
11. Wermuth, C. G. Em The Practise of Medicinal Chemistry; Wermuth, C. G., ed.; Academic Press: San Diego, 1996, p. 243 e 304.
12. Wierzbicki, A. S.; Mikhailidis, D. P.; Wray, R.; Schachter, M.; Cramb, R.; Simpson, W. G.; Byrne, C. B.; Curr. Med. Res. Opin. 2003, 19, 155.
13http://www.scielo.br/scielo.php?pid=S0100-40422007000200033&script=sci_arttext
14http://www.manuaisdecardiologia.med.br/Dislipidemia/Lipid6.htm
15 http://www.contec.org.br/variedades.asp
16http://www.abcs.org.br/portal/mun_car/medico/artigos/1.pdf
domingo, 9 de novembro de 2008
Metabolismo do Colesterol
O colesterol pode ser obtido por síntese endógena (de novo) ou a partir de alimentos ingeridos na dieta. Um adulto saudável produz cerca de 800mg de colesterol por dia, o que corresponde a 70% do colesterol total. O colesterol é principalmente sintetizado no fígado e no intestino delgado. Mas o organismo aproveita também o colesterol proveniente dos alimentos: quando o colesterol chega no intestino delgado, ele é transportado por quilomícrons para o fígado pela via sangüínea e é incorporado às células através de endocitose mediada por receptores em fossas cobertas por clatrina na membrana plasmática. A vesícula assim formada se funde com um endossoma, formando um lisossoma que hidrolizará os constituintes do quilomícron, liberando colesterol que poderá então ser usado pela célula.
O quilomícron é uma lipoproteína de muito baixa densidade (98% de lipídios), que contém um centro hidrofóbico, composto por triglicerídeos e ésteres de colesterol, envolto por moléculas anfipáticas (fosfolipídios, apoproteínas e colesterol) que tornam o quilomícron hidrossolúvel.
 A síntese endógena do colesterol ocorre no citossol e no retículo endoplasmático. Todos os carbonos do colesterol são provenientes da acetil-CoA. A via de síntese do colesterol envolve dezenas de reações que se resumen basicamente na formação de compostos com 5 carbonos seguida pela polimerização destes compostos e a sua ciclização. Esta via utiliza NADPH como agente redutor e consome 18 ATP por molécula de colesterol formada: é uma via redutora com grande consumo de energia.
A síntese endógena do colesterol ocorre no citossol e no retículo endoplasmático. Todos os carbonos do colesterol são provenientes da acetil-CoA. A via de síntese do colesterol envolve dezenas de reações que se resumen basicamente na formação de compostos com 5 carbonos seguida pela polimerização destes compostos e a sua ciclização. Esta via utiliza NADPH como agente redutor e consome 18 ATP por molécula de colesterol formada: é uma via redutora com grande consumo de energia. Etapas principais da via:
1- Duas moléculas de acetil-CoA se condensam formando acetoacetil-CoA, que enseguida reage com outra molécula de acetil-CoA produzindo 3-hidroxi-3-metilglutaril-CoA (HMG-CoA). Estas duas reações ocorrem no citossol e são catalisadas pelas enzimas tiolase e HMG-CoA sintase, respectivamente.
2- A HMG-CoA é reduzida por 2 NAPDH originando mevalonato, um composto de 6 carbonos. Esta reação é catalisada pela HMG-CoA redutase, localizada na membrana do retículo endoplasmático, e é a reação limitante da síntese de colesterol. A HMG-CoA redutase é regulada por meca nismos de fosforilação reversível dependente de hormônios (o glucagon fosforila a enzima inativando-a, enquanto que a insulina a desfosforila ativando-a); por efeitos na transcrição (o colesterol inibe a síntese da redutase); e por inibição pelo própio produto mevalonato.
nismos de fosforilação reversível dependente de hormônios (o glucagon fosforila a enzima inativando-a, enquanto que a insulina a desfosforila ativando-a); por efeitos na transcrição (o colesterol inibe a síntese da redutase); e por inibição pelo própio produto mevalonato.
3- A seguir o mevalonato sofre duas fosforilações, à custa de 3 ATP, e uma descarboxilação, originando isopentenil-pirofosfato (5C).
4- Seis moléculas de isopentenil-pirofosfato sofrem reações de transferência e redução por NAPDH, liberando PPi e produzindo finalmente um composto de 30 carbonos, o esqualeno. Todas estas reações são catalisadas por enzimas presentes na membrana do retículo endoplasmático.
5- O esqualeno sofre oxidação e ciclização gerando lanosterol. A etapa final da via envolve vinte reações onde o lanosterol (30C) é finalmente convertido em colesterol (27C), removendo 3 grupos metila, reduzindo a dupla ligação da cadeia lateral e movimentando-a no interior do anel de lanosterol.


O colesterol presente no organismo pode ter vários destinos diferentes: fazer parte de membranas biológicas; ser transportado por lipoproteínas para outros tecidos; ser precursor de ácidos (sais) biliares; formar hormônios esteróides; ser precursor da vitamina D e auxiliar no metabolismo de vitaminas lipossolúveis.
Por ser uma molécula anfipática (possuir uma parte hidrofílica e outra hidrofóbica), o colesterol é um componente estrutural importante de membranas, influenciando a sua fluidez. Quanto mais colesterol presente na membrana, mais rigida ela é. Recentemente, o colesterol tem sido relacionado a processos de sinalização celular. Sabe-se também que ele reduz a permeabilidade da membrana plasmática aos íons de hidrogênio e sódio.
Para ser transportado no sangue, o colesterol é esterificado a uma molécula de ácidos graxos para aumentar a sua hidrofobicidade e depois empacotado por uma lipoproteína.
Ácidos Biliares
Os ácidos biliares são esteróides di- ou triidroxilados, produzidos no fígado a partir de colesterol. Como em pH fisiológico ocorrem na forma desprotonada, são mais corretamente chamados de sais biliares. Eles podem ser divididos em dois gupos: os primários, sintetizados nos hepatócitos, são os ácidos cólico e quenodesoxicólico; os secundários, formados no intestino pela ação da flora intestinal a partir dos primários, são os ácidos desoxicólico e litocólico.
A conversão do colesterol em ácidos biliares ocorre mediante reações agrupadas em três etapas: remoção das duplas ligações do colesterol, isomerização e hidroxilação. Estas reações consomem NADPH, O2, acetil-CoA e ATP.


 ação chegam ao intestino delgado, a bile é secretada para o duodeno onde tem um papel fundamental de detergente na digestão de lipídios: pelas propiedades anfipáticas dos sais biliares, ela é responsável pela emulsificação dos lipídios, quebrando-os em pequenos pedaços sobre os quais as lipases podem agir, e pela sua solubilização graças à formação de micelas. Os ácidos biliares são também muito importantes para a absorção e o transporte das vitaminas lipossolúveis.
ação chegam ao intestino delgado, a bile é secretada para o duodeno onde tem um papel fundamental de detergente na digestão de lipídios: pelas propiedades anfipáticas dos sais biliares, ela é responsável pela emulsificação dos lipídios, quebrando-os em pequenos pedaços sobre os quais as lipases podem agir, e pela sua solubilização graças à formação de micelas. Os ácidos biliares são também muito importantes para a absorção e o transporte das vitaminas lipossolúveis.Uma parte dos sais biliares perde-se nas fezes (principalmente ácido litocólico), mas a maior parte é reabsorvida no íleo e re-excretada no fígado. A este processo chama-se ciclo entero-hepático dos sais biliares.
Como no organismo humano o anel esteróide não pode ser degradado a CO2 e H2O, a única maneira de excretar o colesterol é através da bile (livre ou sob a forma de sais biliares).
Hormônios Esteróides
Colesterol é o precursor das cinco principais classes de hormônios esteróides: progestagênios, androgênios, estrogênios, glucocorticoides e mineralocorticoides. Estes hormônios regulam uma grande variedade de funções no organismo. Progesterona, um progestagênio, está envolvido na gravidez. Androgênios e estrogênios são necessários para o desenvolvimento de características sexuais secundárias masculinas e femininas, respectivamente. Glucocorticóides são essenciais na resposta ao estresse, promovendo gluconeogênese e a degradação de proteínas e lipídios, enquanto que os mineralocorticóides, principalmente aldosterona, aumentam a reabsorção de sódio e a excreção de potássio e hidrogênio nos rins, aumentando a pressão e o volume sangüíneos.
Estes hormônios são sintetizados nas gônadas (estrogênios, androgênios) ou no córtex das glândulas adrenais (gluco- e mineralocorticóides). As pequenas diferenças estruturais entre eles permitem que interajam com receptores específicos, desencadeiando respostas fisiológicas diferentes.
A conversão de colesterol em hormônios esteróides envolve uma série de hidroxilações que ocorrem na membrana do retículo endoplasmático, mais especificamente no citocromo P450. Todas essas hidroxilações consomem NADPH e O2. Um oxigênio proveniente de O2 forma o grupo hidroxila no substrato e o outro forma água.

O colesterol contém 27 carbonos enquanto que os hormônios esteróides contém somente 21. Assim, a primeira etapa necessária na síntese de hormônios esteróides é a remoção de uma unidade 6C da cadeia lateral do colesterol para formar pregnenolona, a precursora de todos os outros hormônios esteróides.
Etapas da biossíntese dos hormônios esteróides
1- A cadeia lateral do colesterol é hidroxilada nos carbonos 20 e 22, e a ligação entre esses carbonos é subseqüentemente clivada pela desmolase, originando a pregnenolona.

3- A progesterona pode também originar aldosterona mediante 3 hidroxilações e a conversão do grupo metila no carbono 18 em um aldeído.
 4- Finalmente, a progesterona pode também dar origem à androgênios e estrogênios que contém 19 carbonos. A síntese dos androgênios começa com uma hidroxilação no carbono 17 da progesterona seguida por uma clivagem da cadeia lateral contendo os carbonos 20 e 21. A redução do grupo cetônico- 17 do composto assim obtido origina a testosterona. Os estrogênios são sintetizados a partir de androgênios pela perda do grupo metila do carbono 19 e a formação de um anel aromático.
4- Finalmente, a progesterona pode também dar origem à androgênios e estrogênios que contém 19 carbonos. A síntese dos androgênios começa com uma hidroxilação no carbono 17 da progesterona seguida por uma clivagem da cadeia lateral contendo os carbonos 20 e 21. A redução do grupo cetônico- 17 do composto assim obtido origina a testosterona. Os estrogênios são sintetizados a partir de androgênios pela perda do grupo metila do carbono 19 e a formação de um anel aromático.
Vitamina D
A síntese de vitamina D ocorre na pele na presença de luz solar, e é somente dependente dos raios UVB (raios que também causam câncer de pele). A vitamina D, que tem o colesterol como precursor, exerce uma f
 unção importante no controle do metabolismo do cálcio e do fósforo. A sua síntese é influenciada por fatores como a latitude, a estação, a poluição aérea, a área de pele exposta, a pigmentação, a idade, etc. Algumas de suas funções são assegurar o funcionamento correto dos músculos, nervos, coagulação do sangue, crescimento celular e utilização de energia. Tem sido proposto que a vitamina D é também importante para a secreção de insulina e prolactina, resposta imunitária e ao stress, síntese da melanina e para a diferenciação das células da pele e do sangue.
unção importante no controle do metabolismo do cálcio e do fósforo. A sua síntese é influenciada por fatores como a latitude, a estação, a poluição aérea, a área de pele exposta, a pigmentação, a idade, etc. Algumas de suas funções são assegurar o funcionamento correto dos músculos, nervos, coagulação do sangue, crescimento celular e utilização de energia. Tem sido proposto que a vitamina D é também importante para a secreção de insulina e prolactina, resposta imunitária e ao stress, síntese da melanina e para a diferenciação das células da pele e do sangue.Síntese: O colesterol se converte em 7-desidrocolesterol e é fotolisado pela luz ultravioleta originando previtamina D3, que se isomeriza espontaneamente em vitamina D3 (colecalciferol). O colecalciferol se converte em calcitriol (1,25-diidroxicolecalciferol), o hormônio ativo, por reações de hidroxilação no fígado e nos rins. Embora a vitamina D não seja um esteróide, ela se comporta de maneira análoga a eles, ligando-se a um receptor similar aos receptores dos esteróides e formando um complexo que funciona como um fator de transcrição, regulando a expressão de genes.
http://www.ess.ips.pt/escola/Bioquimica/8CLE/GRUPO9/9.4.pdf
http://users.med.up.pt/ruifonte/PDFs/2006-2007/G16_colesterol_ac_biliares.pdf
http://www2.iq.usp.br/docente/henning/sintese.pdf
http://www.ncbi.nlm.nih.gov/books/bv.fcgi?highlight=steroids&rid=stryer.section.3653#3664
http://www.colegiosaofrancisco.com.br/alfa/colesterol/colesterol-6.php
Bayardo e Marzzoco, Bioquímica Básica
terça-feira, 4 de novembro de 2008
O Mecanismo de Transporte do Colesterol e o Papel das Lipoproteínas
 nções que, em conjunto, mantêm a vida do organismo como um todo.
nções que, em conjunto, mantêm a vida do organismo como um todo.O desafio surge da dificuldade de se aliar um mecanismo eficiente de transporte de substâncias, caracterizado pela movimentação de uma massa fluida aquosa, com a necessidade de que nele haja o trânsito de moléculas tão essenciais à vida quanto se mostram serem avessas à água, os lipídios (entre eles, o colesterol). Basta que vejamos a composição do Sistema Circulatório estruturado no transcorrer do histórico filogenético humano, para que possamos entender o aparente paradoxo encerrado por essa questão. Simplesmente, mais de 70% do tecido circulatório (sangue e linfa) é composto de água. E os lipídeos têm que entrar aí de alguma maneira.
Que truque possuíam, então, os seres ancestrais do Homem para que fossem selecionados de forma positiva pela natureza? Ora, como fizeram os seres vivos para findar o impasse: água como veículo de transporte X moléculas hidrofóbicas necessitando serem transportadas para todos os tecidos? Bom, a resposta vem com o advento de toda uma maquinaria especial para o transporte dessas moléculas, maquinaria essa que, óbvio, coexistiu e aperfeiçoou-se ao longo do trilhar da evolução e do histórico filogenético desses seres vivos, até que se chegasse ao modelo que hoje verificamos na espécie humana...
As Lipoproteínas.
O protagonista responsável pela transposição dessa aparente barreira é um conjunto de moléculas denominadas genericamente como
 Lipoproteínas. Elas compõem a química não só do sangue, mas, como poucos sabem, também da linfa. São representadas pelo HDL (High Density Lipoproteins), LDL (Low Density Lipoproteins), VLDL (Very Low Density Lipoproteins), IDL (intermediate Density Lipoproteins) e os Qilomícrons. Suas designações, com exceção dos Quilomícrons, são atribuídas em consonância com suas densidades, sendo que aquelas que possuem uma quantidade maior de lipídeos apresentarão uma menor densidade e mais danos podem causar à integridade dos vasos tanto sangüíneos quanto linfáticos dos indivíduos que evidenciam uma quantidade exacerbada de suas concentrações.
Lipoproteínas. Elas compõem a química não só do sangue, mas, como poucos sabem, também da linfa. São representadas pelo HDL (High Density Lipoproteins), LDL (Low Density Lipoproteins), VLDL (Very Low Density Lipoproteins), IDL (intermediate Density Lipoproteins) e os Qilomícrons. Suas designações, com exceção dos Quilomícrons, são atribuídas em consonância com suas densidades, sendo que aquelas que possuem uma quantidade maior de lipídeos apresentarão uma menor densidade e mais danos podem causar à integridade dos vasos tanto sangüíneos quanto linfáticos dos indivíduos que evidenciam uma quantidade exacerbada de suas concentrações.Por intermédio da microscopia eletrônica de transmissão e de varredura, além de outros métodos de estudo compositivo da matéria, verifica-se sua estruturação anatômica, que, aliás, assemelha-se àquela aplicada ao estudo das Membranas Plasmáticas, uma vez que ambos possuem uma natureza lipoproteica. Observe o esquema a seguir:

Como se vê, as lipoproteínas possuem uma capa periférica hidrossolúvel, de natureza fosfolipídica, com proteínas mergulhadas nessa superfície. A essas proteínas hidrossolúveis dá-se o nome de Apoproteínas ou Apolipoproteínas. Elas são peças-chave para a solubilização dos lipídios, o que possibilita seu efetivo transporte via plasma sangüíneo, bem como sua identificação e destinação correta para cada célula-alvo. Como ocorrem com as proteínas de Membrana Plasmática, elas podem ser classificadas como Intrínsecas (integrais) se transpassarem de um lado a outro da superfície fosfolipídica , ou Extrínsecas (periféricas) se apenas repousarem sobre essa superfície. No centro, há um núcleo ou “core”, onde residem os lipídios mais hidrofóbicos, dado a impossibilidade de interação com o meio aquoso nessa região.
Infere-se, pois, que quanto mais hidrofóbica ou apolar for a molécula, mais ao centro desse complexo ela estará e, por óbvia conclusão, quanto mais hidrofílica ou mesmo anfipática ela o for, encontrar-se-á mais na periferia dessa estrutura. Justifica-se assim o fato de os triglicerídeos e os ésteres de colesterol estarem mais ao centro. É necessário salientar que o colesterol livre compõe tanto a superfície da molécula, conferindo-lhe rigidez, como a parte intermediária entre o núcleo apolar e a superfície fosfolipídica, como se vê no esquema abaixo:

As diferenças primordiais entre cada lipoproteína estão no volume e no tipo majoritário de lipídios encontrado em cada uma delas, na natureza e na quantidade de suas apoproteínas. Veja a tabela a seguir:
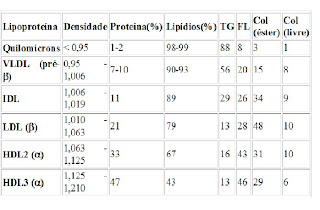 Sendo: TG = triglicerídeos; Col = Colesterol; FL = Fosfolipídeos
Sendo: TG = triglicerídeos; Col = Colesterol; FL = Fosfolipídeos
Como já foi dito, veja que a relação entre lipídeo e densidade mostra-se, de fato, inversamente proporcional. E, de posse desses dados, conclui-se que os Quilomícrons possuem o maior valor em massa de lipídeos, seguido por VLDL, IDL, LDL e, finalmente, o HDL. Os quilomícrons são também os mais volumosos, seguido do VLDL, o que diminuem ainda mais suas densidades e o que dá a eles a capacidade de turvar o plasma sangüíneo quando em excesso na circuitaria sangüínea e linfática.
A Dinâmica do Transporte do Colesterol (acompanhe o texto com o auxílio da figura abaixo)
 Após a ingestão de um alimento rico em lipídeos, os Quilomícrons produzidos pela mucosa intestinal recepcionam e englobam em seus núcleos (ou “core”) os triglicerídeos provenientes da dieta. Isso possibilita ao organismo a absorção dos lipídios via Circulação Linfática, uma vez que, por serem muito grandes, os Quilomícrons não ingressam nos capilares sangüíneos. Note que, por não seguirem a circulação porta-hepática, cujo primeiro destino é o fígado, os lipídios podem primeiro suprir as necessidades de armazenamento dos adipócitos.
Após a ingestão de um alimento rico em lipídeos, os Quilomícrons produzidos pela mucosa intestinal recepcionam e englobam em seus núcleos (ou “core”) os triglicerídeos provenientes da dieta. Isso possibilita ao organismo a absorção dos lipídios via Circulação Linfática, uma vez que, por serem muito grandes, os Quilomícrons não ingressam nos capilares sangüíneos. Note que, por não seguirem a circulação porta-hepática, cujo primeiro destino é o fígado, os lipídios podem primeiro suprir as necessidades de armazenamento dos adipócitos.
A circulação linfática ganha o sistema sangüífero via Ducto Torácico, vaso linfático que, normalmente, desemboca na altura da anastomose entre as veias Julgular Interna Esquerda e Axilar Esquerda, levando a linfa recém-chegada ao átrio direto do coração, juntamente com o sangue. Os Quilomícrons absorvidos na parede entérica entram, agora, em contato com o HDL sangüíneo, que os transfere duas apoproteínas essenciais para a liberação de seus triglicerídeos nos adipócitos, as Apo-C2 e Apo-E.
A Apo-C2 é o elemento discriminante dos Quilomícrons pelos adipócitos, porque aciona a enzima Lípase-lipoproteica ou Lipoproteína Lípase (LPL), a qual hidrolisa os tri-acil-gliceróis (triglicerídeos) em glicerol e ácidos graxos livres, subjacentemente ao tecido adiposo. Ele os capturam e os restaura em triglicerídeos para armazenagem. O mesmo ocorre com o VLDL (explicado mais adiante), também possuidor de Apo-C2.
Aos Quilomícrons resultantes da dinâmica de entrega de ácidos graxos para os adipócitos, isto é, Quilomícrons com baixo conteúdo de triglicerídeos, é dado o nome de Quilomícrons Remanescentes. Findada a sua utilidade, os Quilomícrons Remanescentes são absorvidos pelos hepatócitos, que metabolizam os conteúdos restantes de lipídios. Sua identificação pelo fígado ocorre pelo reconhecimento da Apo-B48 pelas células hepáticas, que o capturam assim que a identificação se estabelece. A Apo-E também tem esse papel.
O principal lipídio metabolizado pelos hepatócitos nessa fase é o colesterol proveniente da dieta, que tem como principais destinos: a excreção como ácido biliar ou como colesterol livre na bile, ajudando na emulsificação de lipídios ingeridos, durante o processo de digestão.
Prova-se, assim, que o colesterol proveniente da dieta pouquíssimo altera os padrões de colesterolemia sangüínea, dado que praticamente todo aquele absorvido permanece na composição dos Quilomícrons Remanescentes, sendo, após metabolização hepática, secretados na bile. Por isso, diz-se que os padrões de hipercolesterolemia não advêm do consumo direto de colesterol da dieta, mas sim do processamento endógeno de outros lipídios consumidos e, no fígado, transformados em colesterol e secretados para a corrente sangüínea.
No fígado, ocorre a produção de colesterol e de triglicerídeos todas as vezes que há um aumento considerável da concentração de Acetil-CoA, por isso, tanto o consumo exagerado de lipídios como o de açúcares é maléfico para quem tem grande tendência à hipercolesterolemia, já que ambos originam Acetil-CoA em transformações metabólicas. Os lipídios endógenos produzidos (colesterol e tri-acil-glicerol) são lançados à corrente sangüínea pela lipoproteína VLDL, possuidora da Apo-B100, além de outras.
Semelhantemente ao que ocorre com os Quilomícrons, o VLDL recebe do HDL as Apo-C2 e Apo-E. Assim, há o mesmo reconhecimento com os adipócitos - já citado – resultando na ativação da Lipoproteína Lípase, com sua mais que importante ação de trâmite lipídico entre lipoproteína e tecido adiposo. Ocorre um novo armazenamento de tri-acil-glicerol no adipócito, permanecendo o VLDL com o colesterol.
Sem os triglicerídeos compondo o VLDL, resultando, então, em uma diminuição de lipídios nessa estrutura, ela perde tamanho e fica mais densa, conforme explicado anteriormente. Nisso se constituem os IDL, também chamados de VLDL Remanescentes. A eles é dado o destino de: (I) ou o de devolverem ao HDL as Apo-C2 e Apo-E, mesmo porque não há mais triglicerídeos no seu interior a entregar, tornando-se desnecessário a permanência da Apo-C2 em sua estrutura (dessa forma, o HDL poderá doar novamente para outro VLDL essas apoproteínas, reiniciando o ciclo); (II) ou o de serem recolhidos pelo fígado, uma vez que possuem Apo-E, que é reconhecida pelo hepatócito como sinal de “alvo de captura” para metabolizações diversas.
Trabalhando com a hipótese numero “I”, após a devolução das apoproteínas, o IDL recebe do HDL ésteres de colesterol, aumentando seu conteúdo de lipídio e, por isso, diminuindo sua densidade. Surge o LDL. Como foi derivado do IDL, o LDL possui uma apoproteína denominada Apo-B100 e muito colesterol para ser repassado aos tecidos, preferencialmente àqueles que produzem hormônios sexuais (Gônadas e Supra-Renais), que têm como precursores o colesterol. Eis aí uma de suas maiores importâncias, além de outras citadas adiante.
Como as células componentes das gônadas e das supra-renais já têm uma capacidade elevada de produção desse composto, sua concentração no interior hialoplasmático é regulado pela forma com que o colesterol presente no LDL é absorvido. A existência de um receptor para a Apo-B100 no glicocálix dessas células é fundamental nesse controle, pois, no momento de encaixe Apo-B100/receptor, há a internalização do complexo receptor/lipoproteína. Se essas células não estiverem precisando de suprimento de colesterol, ela retira o receptor da membrana, havendo acúmulo de LDL no plasma sangüíneo (embora o fígado também reconheça a Apo-B100) à aumenta-se a deposição de LDL na parede dos vasos, podendo gerar doenças cardiovasculares graves.
Como se vê, o HDL é importantíssimo para a manutenção da homeostase dessa dinâmica de trânsito lipídico. Além do mais, estudos mostram que valores elevados dessa lipoproteína representam êxito na retirada de LDL fixados nas paredes de vasos da circuitaria sangüífera, pois captura o colesterol livre presente em sua composição, podendo esterificá-lo por meio de uma enzima denominada Lecitina Colesterol-Acil-Transferase (LCAT - lê-se licat) e incorporar esses ésteres. Depois, como mostrado acima, ele transfere estes ésteres para VLDL circulantes (não depositados em paredes vasculares), transformando-o em LDL, como supra-citado. Isso favorece o consumo desse excesso pelo Fígado e pelas células das Supra-Renais e das Gônadas, no momento em que houver necessidade. O HDL ainda pode ser captado pelo Fígado e ter seu colesterol excretado na forma de ácidos biliares e colesterol livre na bile, a exemplo do que ocorre com o colesterol presente em Quilomícrons. É por tudo isso que o HDL é vulgarmente e incorretamente chamado de “colesterol” bom! Mas, de fato, corresponde em um excelente agente do feedback lipídico sangüíneo. E, por último, como ainda não foi dito, o HDL é produzido unicamente pelo fígado e possui sua concentração consideravelmente elevada em indivíduos com hábitos saudáveis e que ingerem regularmente os chamados lipídios insaturados, presentes, por exemplo, no azeite extra virgem.
Quadro-Resumo

Bibliografia:
http://www.geocities.com/CapeCanaveral/Launchpad/9071/Lipoprot.html
http://www.geocities.com/bioquimicaplicada/resumoslipoproteinas.htm



